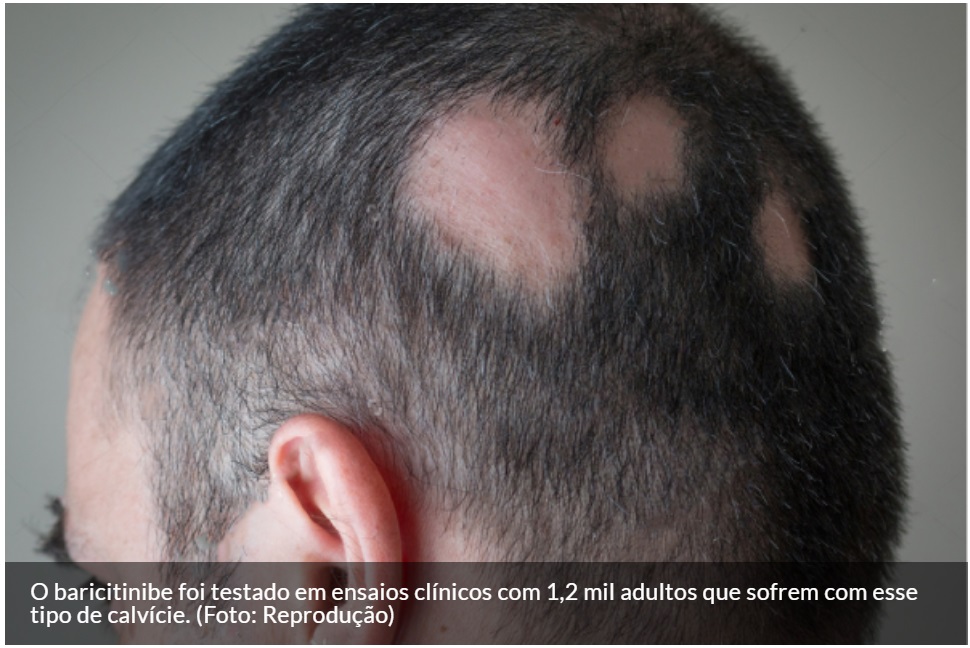
A Food and Drug Administration (FDA) dos EUA aprovou os comprimidos orais de Olumiant (baricitinibe) para tratar pacientes adultos com alopecia areata grave, um distúrbio que geralmente aparece como calvície irregular e afeta mais de 300.000 pessoas nos EUA a cada ano.
A ação marca a primeira aprovação do FDA de um tratamento sistêmico (ou seja, trata todo o corpo em vez de um local específico) para alopecia areata, que é uma doença inflamatória que atinge também a atriz Jada Pinkett Smith, gera uma perda localizada de cabelo ou pelos em diversas áreas do corpo.

“O acesso a opções de tratamento seguras e eficazes é crucial para o número significativo de americanos afetados pela alopecia grave”, disse Kendall Marcus, MD, diretor da Divisão de Dermatologia e Odontologia do Centro de Avaliação e Pesquisa de Medicamentos da FDA. “A aprovação de hoje ajudará a atender a uma necessidade significativa não atendida de pacientes com alopecia areata grave.”
A alopecia areata, comumente referida como apenas alopecia, é um distúrbio autoimune em que o corpo ataca seus próprios folículos capilares, fazendo com que o cabelo caia, muitas vezes em tufos. Olumiant é um inibidor da Janus quinase (JAK) que bloqueia a atividade de uma ou mais de uma família específica de enzimas, interferindo na via que leva à inflamação.
A eficácia e a segurança de Olumiant na alopecia areata foram estudadas em dois estudos randomizados, duplo-cegos e controlados por placebo (Ensaio AA-1 e Ensaio AA-2) com pacientes que tiveram pelo menos 50% de perda de cabelo no couro cabeludo, conforme medido pela Gravidade da Alopecia Tool há mais de seis meses. Os pacientes nesses ensaios receberam um placebo, 2 miligramas de Olumiant ou 4 miligramas de Olumiant todos os dias. A medida primária de eficácia para ambos os ensaios foi a proporção de pacientes que atingiram pelo menos 80% de cobertura capilar do couro cabeludo na semana 36.
No Ensaio AA-1, 22% dos 184 pacientes que receberam 2 miligramas de Olumiant e 35% dos 281 pacientes que receberam 4 miligramas de Olumiant alcançaram uma cobertura capilar adequada, em comparação com 5% dos 189 pacientes que receberam placebo. No Ensaio AA-2, 17% dos 156 pacientes que receberam 2 miligramas de Olumiant e 32% dos 234 pacientes que receberam 4 miligramas de Olumiant alcançaram uma cobertura capilar adequada, em comparação com 3% dos 156 pacientes que receberam placebo.

Os efeitos colaterais mais comuns associados ao Olumiant incluem: infecções do trato respiratório superior, dor de cabeça, acne, colesterol alto (hiperlipidemia), aumento de uma enzima chamada creatinina fosfoquinase, infecção do trato urinário, elevações das enzimas hepáticas, inflamação dos folículos pilosos (foliculite), fadiga, infecções do trato respiratório inferior, náuseas, infecções fúngicas genitais (infecções por Candida), anemia, baixo número de certos tipos de glóbulos brancos (neutropenia), dor abdominal, zona (herpes zoster) e aumento de peso.
Olumiant não é recomendado para uso em combinação com outros inibidores de JAK, imunomoduladores biológicos, ciclosporina ou outros imunossupressores potentes. Olumiant vem com avisos e precauções, incluindo a recomendação de monitoramento rigoroso para o desenvolvimento de sinais e sintomas de infecção durante e após o tratamento; avaliação de pacientes para infecção ativa por tuberculose e teste para tuberculose latente antes do tratamento com Olumiant; e o potencial de reativação viral. Além disso, outras advertências e precauções incluem hipersensibilidade (reações alérgicas), perfurações gastrointestinais (lágrimas no estômago ou intestino) e anormalidades laboratoriais, incluindo contagens baixas de glóbulos brancos e vermelhos, elevações de enzimas hepáticas e elevações de lipídios.
Olumiant vem com um aviso em caixa para infecções graves, mortalidade, malignidade, eventos cardiovasculares adversos importantes e trombose.
Olumiant recebeu revisão prioritária e designações de terapia inovadora para esta indicação.
Olumiant foi originalmente aprovado em 2018. É aprovado como tratamento para certos pacientes adultos com artrite reumatóide ativa moderada a grave. Olumiant também é aprovado para o tratamento de COVID-19 em certos adultos hospitalizados.
A FDA concedeu a aprovação do Olumiant à Eli Lilly and Company.
*FDA
GOSTA DE NOTÍCIAS NA PALMA DA MÃO?
ACESSE NOSSOS GRUPOS NA SUA REDE SOCIAL PREFERIDA E RECEBA NOSSAS INFORMAÇÕES